Der Mensch kommt nicht ohne sie aus. Menschliche Kultur ohne sie wäre undenkbar. Jeder ist auf sie angewiesen – aber niemand will die Industrie in seinem Vorgarten haben: Es geht um Rohstoffe.
Ein weites Thema, das in dieser Folge von Gunnar Ries (Mineraloge) und Karl Urban (Geologe) ergründet wird, heruntergekocht und moderiert von Faldrian.
Titelbild: Andreas Feininger / Library of Congress Prints and Photographs Division, Farm Security Administration – Office of War Information Collection / Wikimedia Commons / gemeinfrei
Grafiken
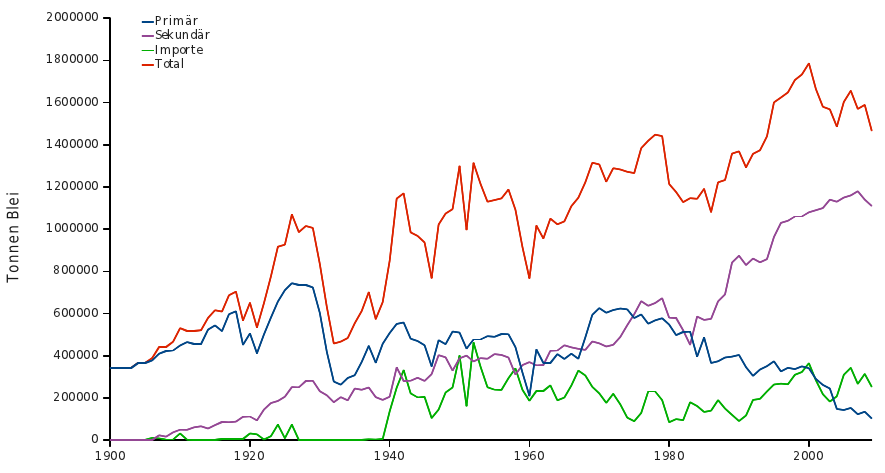
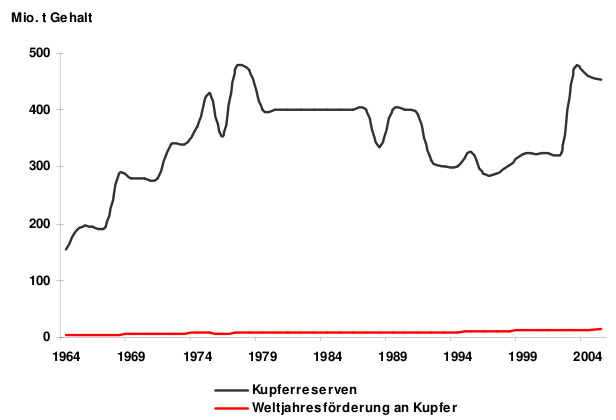
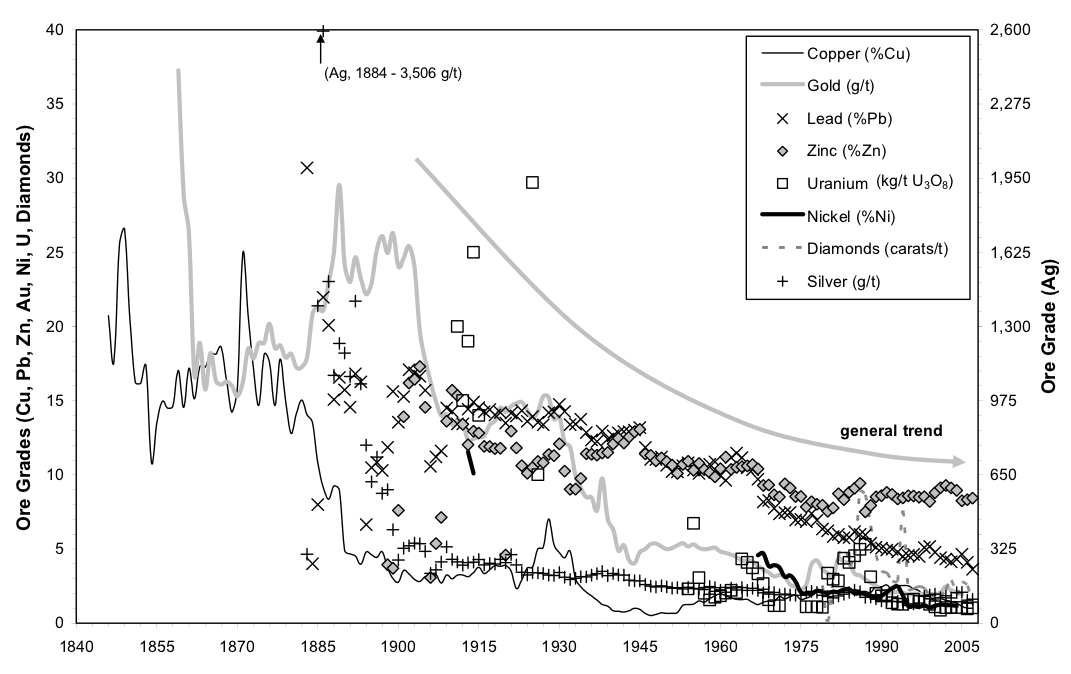
Fakten
- 1970 förderten Bergwerke noch halb so viel Metalle 1999: Da waren es 9,6 Milliarden Tonnen [1]
- Energiebedarf des globalen Bergbaus in späten 1990er Jahren: 10% des Weltenergieverbrauchs [1]
- SO2-Emissionen des globalen Bergbausin späten 1990er Jahren: 13% der globalen Emissionen [1]
- Bis 2050 dürften Bergwerk 2-3 mal mehr Material fördern als heute [2]
- Anders als erzählt, passierte der erste Nachweis von Aluminium noch ohne elektrolytische Verfahren
- Das von Johannes Gutenberg verwendete Metall heißt Antimon. Wir sprechen von Antimonit – das ist das Mineral, aus dem Antimon gewonnen wird.
Quellen
[1] A. Whitmore: The emperors new clothes: Sustainable mining?, Journal of Cleaner Mining, 2006
[2] P. Laznicka: Giant Metallic Deposits: Future Sources of Industrial Metals, Springer, 2010
Links
- Gunnar Ries: Mente e Malleo
- Faldrian: Twitter / Blog
- WP: Rohstoffe
- WP: Bergbau
- WP: Kupfer
- WP: Kupfersteinzeit
- WP: Quecksilber
- WP: Bronzen
- WP: Bronzezeit
- WP: Zinn
- WP: Eisen
- WP: Eisenzeit
- WP: Blei
- WP: Johannes Gutenberg
- WP: Druckerpresse
- WP: Lettern
- WP: Antimonit / Antimon
- WP: Aluminium
- WP: Lithium
- WP: Tritium
- WP: Alchemie
- Amazon: Die Welt der Rohstoffe
- WP: Lagerstätte
- WP: Magmatismus
- WP: Fraktionierung / Fraktionierte Kristallisation
- WP: Merensky-Reef (Platinlagerstätte)
- WP: Überkritischer Zustand
- WP: Gang
- WP: Geoden
- WP: Kieselsäure
- WP: Nickel
- WP: Sudbury-Lagerstätte / -Becken
- WP: Reichweite
- WP: Peak Oil (Erdölfördermaximum)
- KSL: Kupfer Schiefer Lausitz
- WP: Seltene Erden
- WP: Mountain Pass Mine
- WP: Fracking, Hydraulic Fracturing
- AG006 Fracking
- WP: Urban Mining
- WP: Bioleaching
- WP: Lake George, Uganda
- AG009 Faires Gold
- WP: Fairphone
- Mente e Malleo: Macht Windenergie Krebs?
- AstroGeo: Eine Welt ohne Bergwerke: Geht das?
- WP: Mittelozeanischer Rücken
- WP: Asteroid Mining
- National Geographic: Meteorite Beads Oldest Example of Metalwork



Eingangs sei angemerkt, dass ich diesen Podcast sehr schätze, aber bei den einführenden Kapiteln von dieser Episode blutete mein Chemiker Herz.
Die Metalle werden nicht aus dem Erz heraus geschmolzen! Die Metalle (genauer die Metallionen) die zumeist in Form von Oxiden im Erz vorliegen werden zum elementaren Metall reduziert. Die Temperatur die hierfür notwendig ist, wird nur am Rande durch deren Schmelzpunkt bestimmt, entscheidender ist hier die Aktivierungsenergie für die Redoxsreaktion. Der Grund warum sich z.B. das Quecksilber bei relativ niedrigen Temperaturen aus dem Zinnober (Quecksilbersulfid) gewinnen lässt liegt an der schwachen Hg-S-Bindung. Daher zersetzt sich HgS auch schon bei 580°C thermisch bevor es schmilzt.
Nebenbei wird der Kohlenstoff, egal ob Holzkohle oder Steinkohle, nicht nur als Brennstoff zum erzielen der Temperatur sonder auch als Reaktionpartner der selber oxidiert wird in der schon erwähnten Redoxreaktion benötigt.
Lithium ist auch nicht selten in der Erdkruste vorhanden, es hat einen größeren Anteil als z.B. Blei, das Problem ist die Verteilung. Es gibt nur wenige Lagerstätten an dem Lithium in Konzentrationen vorliegt die eine wirtschaftliche Gewinnung ermöglichen.
Bei überkritischem Wasser von “aggressiv” zu sprechen finde ich auch eher unpassend. Das Löslichkeitsvermögen, genauer das Löslichkeitsprodukt, ist für viele Substanzen in überkritischem Wasser schlichtweg um Größenordnungen höher als in flüssigem Wasser.
Ich hoffe Ihr nehmet mir diese Kritik nicht übel.
Macht weiter, es kann gar nicht genug Wissenschaftspodcasts geben!
Gruß aus Köln/Jülich,
Frank
Auch ich schätze diesen Podcast, aber diese Episode war wirklich grausam. Soviele falsche Aussagen!!! Ich konnte sie mir nicht zu Ende anhören. Frank ist ja schon auf die Details eingegangen. Hoffentlich geht es in Zukunft wieder auf dem gewohnten Niveau weiter.
Grüße aus Heilbronn,
Hakan
Danke für eure Kritik, Frank und Hakan. Und Asche auf mein Haupt wegen der recht ungenauen Ausführungen. Tatsächlich hat diese Sendung einen Überblick über ein sehr großes Thema gegeben – daran litt dann die Vorbereitung meinerseits.
Es lohnt sich sicher, das Thema Erzaufbereitung und Metallurgie in einer gesonderten Sendung nochmal genauer (und richtig!) aufzurollen. Vorschläge für gute Gesprächspartner nehme ich gerne entgegen!